Етиология, класификация, клинично представяне, диагностика и лечение на остра миелоидна левкемия.
Съдържание
 Остра левкемия — хетерогенна група клонални
Остра левкемия — хетерогенна група клоналнитуморни заболявания на хемопоетичната тъкан, характеризиращи се с неконтролирано
разпространение, нарушена диференциация и натрупване в костен мозък и
периферна кръв на незрели хемопоетични клетки.
Острата левкемия представлява 2-3% от злокачествените тумори
човек. Честотата на острата левкемия е средно 3-5 случая на
100 000 население. IN В 75% от случаите заболяването се диагностицира възрастни, в 25%
дела — в деца. Средно съотношение на миелоид и лимфоидна остра левкемия
е 6: 1. Имайте възрастни пациенти в над 40 на възраст 80% от случаите
са представени от миелоидни форми, в деца — 80-90% — лимфоидна. Медиана
възраст на пациенти с остра нелимфобластна левкемия — 60-65 години, остър
лимфобластна левкемия — 10 на възраст.
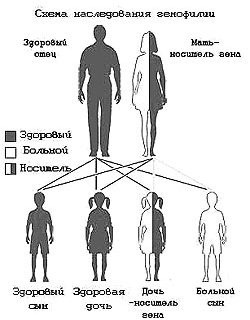
Съществува генетична вероятност да се развие остро
миелоидна левкемия. Има голям брой доклади за семейни дела
заболявания, вероятността от ОМЛ при близки роднини на пациента
три пъти по-висока. Редица вродени състояния могат
увеличаване на вероятността от AML. Най-често това е синдром на Даун, при който вероятността от ОМЛ се увеличава
10 — 18. веднъж.
Някои канцерогени
(туморо-индуциращи агенти) могат да се считат за етиологични фактори
AML, като бензин, тютюнопушене и йонизиращо лъчение. Най-важните
възраст над 65 години е рисков фактор на възраст.
Влияние на индивида
- генетичните характеристики на организма, и също въздействие върху организъм екзогенен
фактори се проявява в развитие на вторична остра миелоидна левкемия,
съставляващи 5-20% от всички случаи на ПМБ. IN по-специално, AML може да се развие в
хора, които преди това са били лекувани с различни схеми на химиотерапия за повод
други злокачествени тумори.
Наличието на предишна фаза в
формата на миелодиспластичен синдром (MDS), която е най-често срещана при възрастен
пациентите също е важен рисков фактор за ОМЛ. Антинеопластичен
химиотерапевтични ефекти, особено при алкилиращи лекарства, антрациклини
и епиподофилотоксини, увеличава вероятността от развитие на вторични
AML / вторичен MDS. Най-високата вероятност от заболяване пада 3-5 години
след химиотерапия. Комбинираното използване на химиотерапия / лъчетерапия също е важно
увеличава риска от вторична AML / вторична MDS. Трябва да се отбележи, че вторичен
левкемия / MDS не се появяват в от всички пациенти, получили противотуморно
лечение.
Острата левкемия е
последица от повреда — мутации — в генетичен материал клоногенен
хематопоетична клетка. IN в резултат на това на настъпва молекулярно ниво
събития, водещи до нарушение на контрола над клетъчен цикъл, промяна
транскрипционни процеси и производство на редица ключови протеинови регулатори. Злокачествен
клетките в AML са миелобласти,
не може да узряване и диференциация в резултатът от нарушеното
генетичен контрол и натрупване
в костен мозък. Клетки на левкемичен клон
пречат на дейността на нормалните клетки, измествайки ги от костен мозък.
IN сега всички остри
левкемията обикновено се разделя на миелоидна и остра лимфобластна левкемия.
Класификацията на СЗО за остра миелоидна левкемия е представена по-долу..
Класификация на СЗО на остра миелоидна левкемия
| Име на подвид | Описание |
| AML с характерни генетични промени |
Имайте болни с такъв подтип на AML обикновено високи нива на ремисия и прогнозата е по-добра в сравнение с AML други подвид. |
| AML с дисплазия няколко кълнове | Този подвид включва пациенти с предшестващ миелодиспластичен синдром (MDS) или миелопролиферативно заболяване (MPD), които отиват до AML. Този подтип на AML е по-често срещан в възрастни хора и има лоша прогноза. |
| AML и Свързани с MDS предишно лечение | Този подвид AML включва пациенти, получили химиотерапия и / или лъчетерапия след от които е възникнала AML или MDS. При тези левкемии може да има характерни промени в хромозоми, прогнозата често е по-лоша. |
| AML, не попадащи под знаците на изброения подвид | Включва AMD подвид, не включен в изброени по-горе. |
Франко-американско-британски
класификация
Френско-американско-британска класификация (FAB)
системата разделя AML на осем подвид, от М0 На M7 въз основа на видове
клетки — предшественици на левкоцити и на падеж на променения
клетки. Определянето на злокачествени клетки се извършва на основата
външни признаци при светлинна микроскопия и / или цитогенетично, разкриващи
лежи в базирани на вариации промени в хромозоми. Имайте различни подтипове на AML
различна прогноза и отговор на лечение. Въпреки ползи от класификацията на СЗО,
FAB система до все още се използва широко. От FAB има осем подтипа
AML.
| Подвид | Име | Цитогенетични промени |
| М0 | Минимално диференциран остра миелоидна левкемия | |
| М1 | Пикантен миелоидна левкемия без съзряване | |
| М2 | Пикантен миелоидна левкемия с узряване на гранулоцитите | t (8; 21) (q22; q22), t (6; 9) |
| М3 | Промиелоцитен, или остър промиелоцитен левкемия (APL) | t (15; 17) |
| М4 | Пикантен миеломоноцитна левкемия | inv (16) (p13q22), del (16q) |
| M4eo | Миеломоноцитна комбинирано с еозинофилия на костния мозък | покана (16), t (16; 16) |
| М5 | Остър монобластичен левкемия (M5a) или остра моноцитна левкемия (M5b) (M5b) | del (11q), t (9; 11), t (11; 19) |
| М6 | Остър еритроид левкемии, включително еритроцитна левкемия (M6a) и много рядко чист еритроидна левкемия (M6b) | |
| М7 | Пикантен мегакариобластна левкемия | t (1; 22) |
| М8 | Остър базофилен левкемия |
Клинична картина
Клиничната картина на острата левкемия се определя от тежестта
основни синдроми:
- Анемични — намаляване на нивата на хемоглобина и
броя на червените кръвни клетки, което се проявява
слабост, намалена работоспособност, сънливост, прояви
сърдечна недостатъчност, сърцебиене,
слабост, задух, бледност на кожата и лигавични, ортостатични
хипотония, вторична ангина и инфаркт на миокарда, с прекъсвания
куцота, клинични признаци на дихателна недостатъчност в болни с хронична
бронхо-белодробни заболявания (ХОББ). - Гранулоцитопеничен — инфекциозни усложнения,
поради намаляване на броя на гранулоцитите в кръв, което се проявява с висока температура и интоксикация и същото
местна клиника (некротизиращ тонзилит, улцерозен стоматит, остеомиелит
челюст след вадене на зъб) или генерализиран (сепсис, инфекциозен ендокардит),
по-често бактериална, инфекция. - Хеморагичен
— кръвоизлив в кожата и лигавици, нос и гингивално кървене,
стомашно-чревни и бъбречно кървене, маточно кървене, увеличено
кървене в време на операцията. - Пролиферативно
— лимфаденопатия, спленомегалия, хепатомегалия, хиперпластичен гингивит,
болка в кости, дисфункция на черепно-мозъчните нерви, главоболие, нарушения
зрение, общо и фокална неврологична
симптоми, главоболие, приапизъм. - Интоксикация
— слабост, намален апетит, загуба на тегло, изпотяване.
Диагностика на остра левкемия
 Първият
Първият
стъпвай в диагнозата е
клиничен кръвен тест чрез вземане на кръвна проба от вени. IN кръвна проба
броя на кръвните клетки (еритроцити, левкоцити и тях подтипове и
също тромбоцити). Когато се намери в клиничен анализ на кръвта повече двадесет%
бластните клетки могат да бъдат диагностицирани с остра левкемия.- В
отсъствие в достатъчно кръв за диагностициране на броя на взривовете и също с
целта на точната проверка на диагнозата с прилагане на допълнителни методи
изследването показва аспирационна биопсия на костния мозък.
Изследването на костния мозък включва изследване на аспират на костния мозък
(анализ на миелограма - цитологично изследване), в в редки случаи се извършва трепанобиопсия
костен мозък за хистологично изследване на костния мозък. - IN
като допълнителни изследователски методи за определяне на възможността за остра
левкемия и се извършват прогностични маркери:
- Цитохимични
изследвания (миелопериксидаза, естераза, гликоген) - Цитогенетични
проучване — идентифициране на хромозомни аномалии, като липсващи или
допълнителни хромозоми в клетки на костния мозък чрез стандартен анализ
метафаза или РИБА
(Флуоресцентен
хибридизация в
ситу — метод, базиран на възможности
хромозомна ДНК (мишена) за свързване при определени условия с малък
ДНК последователности (сонди), допълващи тази хромозомна ДНК. В
присъединяване сондата на флуоресцентното вещество се анализира чрез ДНК неговата
местоположение на клетките в междуфазни клетки). Цитогенетични резултати
проучванията имат както диагностична стойност, така и прогностичен.
| Изход | Отклонения | 5-годишно оцеляване | Честота на рецидиви |
| Благоприятен | t (8; 21), t (15; 17), инв (16) | 70 % | 33 % |
| Задоволително | Не открити, +8, +21, +22, del (7q), del (9q), Нарушения 11q23, всички останали структурни или числени промени | 48 % | петдесет % |
- Молекулярно биологични
изследвания (генетични изследвания се извършват за идентифициране на характеристика
мутации, които могат да повлияят изход от заболяването — например, FLT3 тирозин киназа, гена CD117, отговорен за синтез на рецептори
растежен фактор на стволови клетки с-KIT, гени CEBRA,
BAALC, ERG, NPM1. - Проучване
на туморни клетки на диференциращи антигени (CD) чрез поточна цитометрия (имунофенотипиране).
IN по нататък пациенти с остър
левкемия, се извършват повторни изследвания на костния мозък, за да се
определят ефекта от терапията, пълнотата на постигнатата ремисия и етап от процеса
(ремисия, стабилизация, прогресия).
Клинични етапи и фази на заболяването
- Основен активен
сцена — интервалът от време между първите клинични прояви
заболявания, диагностика и постигане на първата пълна ремисия - Пълна
клинична и хематологична ремисия — броя на бластните клетки в миелограма
намалява по-малко 5%, няма допълнителни левкемични огнища на костния мозък
поражение, докато в периферна кръв не е трябва да има взривни клетки,
брой тромбоцити 100×109 / l, левкоцити 2.5 NS
109 / l, гранулоцити 1.0 NS
109 / l, ниво на хемоглобина 100 g / l.
IN наскоро представи концепцията за цитогенетични и молекулярно биологични
ремисия. - сцена
минимално остатъчно (остатъчно) заболяване. - Рецидив
заболявания (костен мозък, допълнителен костен мозък). - Терминал
сцена.
Лечение
Преди започване на лечение, пълна клинична
преглед на пациента за оценка на състоянието на съпътстваща патология
сърдечно-съдова, дихателна, пикочно-полова система, централна нервна система.
IN тя включва пълен биохимичен кръвен тест, коагулограма, изследване за
хепатит В и С, ХИВ, вируси от херпесната група. Ултразвуково изследване на органи
коремна кухина, рентгенова снимка на гръдния кош / компютър
томография на гръдния кош, ЕКГ / ехокардиография, КТ / ЯМР на главата, преглед
невролог, офталмолог и и т.н. Всичко това е необходимо за правилния избор на лечение и
предотвратяване на усложнения.
Методи на лечение
пациенти с AML зависи от вид заболяване, прогностични фактори, възраст
болни и също съпътстваща патология и може да се подраздели на
потенциално лечебни терапии и поддържаща терапия.
Подкрепяща и
симптоматична терапия
Основата
AML лечението е поддържаща терапия, която включва лечение на интеркурентни инфекции, пикочна киселина
диатеза, заместителна терапия с кръвни съставки и също лечение
съпътстваща патология.
IN основа
поддържаща терапия за пациенти с MDS е заместителна терапия
кръвни съставки. Имайте пациенти с нисък риск от развитие на AML анемия може да бъде
основно клинично значим проблем. Заместителна терапия
облекчава симптомите на анемия и следователно е важно лечение.
Честота
преливането зависи от състоянието на пациента, тежестта на анемията и същото
съпътстваща патология, необходимостта от преливане на компоненти
кръв по време на развитието на кървене от пациент. Резултатът от заместващата терапия
е повишаване на нивата на хемоглобина, което показват проучванията,
има положителна корелация с показател за качеството на живот.
Преливане
тромбоцитната маса се извършва през в случаите, когато броят на тромбоцитите
изключително ниско и / или животозастрашаващо кървене. С развитие
коагулопатии (нарушения в системата за съсирване на кръвта, например намаляване на нивото
фибриноген или протромбинови комплексни фактори) извършват заместване
терапия с компоненти на кръвната плазма или
рекомбинантни лекарства (новосевен, протромбоплекс и и т.н.)
Потенциално лечебни терапии
-
 За контрол на симптомите на заболяване или за излекуване на ОМЛ в младите пациенти използват
За контрол на симптомите на заболяване или за излекуване на ОМЛ в младите пациенти използват
интензивна химиотерапия с цел максимално унищожаване на клонинга на патологични
клетки и постигнете дългосрочна ремисия. Този метод на лечение има
значителни странични ефекти като косопад, стоматит
устна кухина, гадене, повръщане, разхлабени изпражнения. В допълнение към тези странични
явления, химиотерапията има неблагоприятен ефект и на здрави
клетки, което изисква дълъг престой в състояния на хематологични
клонове. IN този път пациентът се подлага на трансфузия на еритроцити и
тромбоцитна маса, антибактериални лекарства се предписват за борба
инфекция. Ако индукционната химиотерапия осигурява адекватен контрол върху
патологични клетки (състояние на ремисия), тогава възстановяване на нормалното
кръвните клетки трябва да започват от в продължение на няколко седмици. Въпреки това, дори в дела
успешно лечение, болестта може да се върне — повтарят. - Единственият
известен метод на лечение, който може да излекува повечето пациенти с AML,
е трансплантацията на алогенен (донорен) хемопоетичен ствол
клетки. Трябва да има имайте предвид, че това е сложна процедура, свързана с риск
рано и късни усложнения. Резултатът от лечението зависи от степента на съвместимост (HLA-съвместимост) на донора и търпелив
(получател) и също от наличие на подходящи донорни клетки (наличност
съвместими кръвни братя и / или сестри, наличие на банка донори). Така
начин, има строги указания и противопоказания за този вид лечение:
подходящ е за онези случаи, когато пациентите в в състояние да прехвърля
трансплантация на стволови клетки и имат подходящ донор и отговори на химиотерапевтично лечение. - Проучване
механизми за развитие на MDS / вторичен AML, предприети през последните години показаха,
че тази патология се характеризира с хиперметилиране на промоторния регион
някои туморни супресорни гени, което води до «мълчание» тези гени и
пролиферация на туморни клетки и трансформация в AML. На въз основа на това знание
са разработени така наречените хипометилиращи агенти, които насърчават
хипометилиране на ДНК, причиняващо по-ранна експресия «изключен» гени.
IN Май 2004 г. Офис
САЩ на контрол над храна и Лекарства (Food and Drug Administranion, FDA) е издал разрешение за приложение
инжекционно лекарство азацитидин (Vaidaza) за лечение на всички видове MDS. IN RF
лекарството е одобрено за заявление в 2010 г. година в включително за лечение на MDS и AML. Резултатите от изследването показаха това
Азацитидин значително удължава живота на пациентите с остра миелоидна левкемия,
които не са показана / интензивна трансплантация на стволови клетки
химиотерапия. IN проучвания показват, че оцеляването на пациенти с ОМЛ без съвременно лечение е 1,6
месеци в тогава докато азацитидин увеличава продължителността на живота при ОМЛ
на 11.1 месеци с благоприятен
профил за сигурност. Освен това,
лекарството, с достатъчна квалификация на медицинския персонал, може
кандидатстват амбулаторно.
Според Руски протоколи, лечение на пациенти с ОМЛ, които не са
подходящ за интензивно
химиотерапия и вторичната AML се извършва с ниски дози цитарабин и / или с
използване на поддържаща терапия [един]. Такава терапия
подобрява качеството на живот на пациентите, но не увеличава продължителността на тяхното живот
в сравнение с естествен ход на заболяването. IN тогава време като приложение
азацитидин у тази категория пациенти може радикално да промени курса
заболявания (таблица 1).
маса
1. Средна обща преживяемост в Пациенти с ОМЛ в зависимост от терапия (непряка
сравнителни данни).
| Без лечение | Поддържаща терапия | Ниски дози цитарабин | Азацитидин | |
| AML, в сила на звука брой AML с броят на взривовете в миелограма 20-30% | 1.6 | 13.4 | 17,0 | 24.5 |
Средна преживяемост на пациенти с AML (20-30% взривове),
получаването на азацитидин се увеличава до 24.5 месеци. В същото време различията в групата
азацитидин c групи за поддръжка и ниски дози цитарабин
статистически значим (p = 0,045), независимо от възраст или кариотип, и
допълнителните месеци за живот са 11.1 и 7,5 съответно (медиана
оцеляване в групата на поддържащата терапия е 13,4 и в група от ниски
дози цитарабин — 17,0 месеца) (анализ на данни от фаза III проучване AZA-001) [2]. След 2 години 50,8% от пациентите са били живи през група
азацитидин, който в 2 пъти повече от групи за сравнение (26,2%). За
сравнения — пациенти с AML, не получавайки съвременна терапия (естествена
ход на болестта) умират в над 7 седмици от диагноза.
 За пациенти с AML, което не е така
За пациенти с AML, което не е така
показана интензивна химиотерапия / трансплантация на стволови клетки, лечение
азацитидин може да е единственият агент, който удължава живота и
помага за постигане на дългосрочна ремисия. IN проучване AZA-001 в групата на азацитидин за отговор на терапия
(Критерии на IWG
2000) достигна 29% от пациентите (пълни и частичен отговор), y 49% — постигнати
хематологично подобрение. Разлики с групи за сравнение («поддържащи
терапия», «ниски дози цитарабин») са статистически значими (5 и 12%, 31 и 25%
съответно). Време до прогресията на заболяването е била 14,1 месеца през
група «азацитидин» и 8,8 месеца в групи за сравнение (p = 0,047). Продължителност
хематологичният отговор е 13,6 месеца на азацитидин в сравнение с
5.2 месеца нататък традиционно използвана терапия (p = 0,002).
Имайте пациенти с MDS и AML получаване
лечение с азацитидин, има по-голяма вероятност за независимост от
трансфузия на еритроцити: 45% от пациентите са станали независими от
кръвопреливане, в тогава време като за традиционни режими — само 11% (стр < 0,0001).
По този начин, лечение с азацитидин при пациенти с ОМЛ (20-30% от бластите)
придружени от не само по-висока продължителност на живота и обща сума
честотата на ремисии в сравнение с поддържаща грижа и ниски дози цитарабин,
но и по-високи нива на хематологично подобрение и независимост от
преливане. Имайте пациенти с Високорискова MDS терапия с азацитидин
придружен от увеличаване на времето до трансформация в AML (17,8 месеца срещу 11.5 месеци, стр<0,001).
Азацитидин е включен в международни протоколи за лечение
пациенти с миелодиспластичен синдром и AML в пациенти над 60 години на възраст.
САЩ: в насоки за AML лечение от Националния
Ракова мрежа (Национален Рак Изчерпателно Мрежа, NCCN, САЩ) (2010) азацитидин се препоръчва за употреба при
пациенти над 60 години години, не кандидати за висока доза
химиотерапия. Препоръки от високо ниво на доказателства.
ДА СЕ
нежелани явления от 3-4 градуса, развиващи се на по време на лечение с азацитидин,
включват хематологични (71,4%), включително тромбоцитопения (85%), неутропения
(91%) и анемия (5